®CANCERNEO
تحديد المستضدات الجديدة لتصميم لقاح مضاد للسرطان الشخصي

تتطور عملية تخصيص علاج السرطان بسرعة كبيرة. تطوير لقاح مضاد للسرطان شخصي هو استراتيجية واعدة لعلاج السرطان.
تقدم الخلايا الجسمية باستمرار الببتيدات على سطحها، مما يشير إلى الحالة الحالية للخلية. يمكن للخلايا المناعية التعرف على ما إذا كانت الخلية تقدم ببتيدات طبيعية أم غير طبيعية واستخدام هذه المعلومات لتحديد والقضاء على الخلايا المعيبة. تنشأ الببتيدات غير الطبيعية، المعروفة باسم المستضدات الجديدة ، من طفرات الحمض النووي في خلايا الورم وتُعد أهدافًا للعلاج باستخدام لقاحات شخصية.
يمكن لـ ®CancerNeo من CeGaT تحليل جينوم ورم المريض لاكتشاف الطفرات الخاصة بالورم (الجسدية)، وتحديد أنواع HLA، وتوقع المستضدات الجديدة. يتم تأكيد تعبير هذه المستضدات الجديدة من خلال تسلسل RNA الكامل (الترانسكريبوم) من نفس عينة الورم. بالتالي، يوفر ®CancerNeo الرؤى اللازمة لتصميم لقاحات السرطان الشخصية - وهي أداة قوية لتعزيز استجابة الجهاز المناعي لخلايا السرطان.
ما نقدمه مع هذه الخدمة
تقييم مفصل
للطفرات الجسدية في أكثر من 700 جين
تحليل شامل
يستند إلى ®ExomeXtra لـ CeGaT
تقرير ثانوي
مع اختيار الببتيدات لصياغة لقاح
المستضدات الجديدة ذات الصلة
للفصائل HLA الفئة I و HLA الفئة II
تفاصيل الخدمة
تسلسل الإكسوم الكامل للأنسجة الورمية / الطبيعية باستخدام ExomeXtra® لـ CeGaT. تقييم مفصل للطفرات الجسدية المكتشفة في أكثر من 700 جين ذي أهمية للأورام والاندماجات في أكثر من 30 جين.
تقرير طبي يتضمن
- قائمة موثقة من الطفرات ذات الأهمية العلاجية المحتملة.
- خيارات العلاج استنادًا إلى الطفرات الجسدية.
- تحديد للتحميل المتعدد للورم/ MSI والتنبؤ بالاستجابة للعلاج / تحديد درجة النقص في إعادة التركيب الهملوجي (HRD).
- الكشف عن الطفرات في عدد النسخ لـ CNVs.
- قائمة بجميع الأدوية المؤهلة والتي تمت الموافقة عليها من قبل EMA و / أو FDA والتي يمكن اكتشاف مؤشراتها المقابلة في الورم.
- تحديد للطفرات الجينية المؤثرة على التمثيل الغيني لبعض الأدوية الورمية أو المخدرات التخديرية.
- تقييم الأدلة على وجود CHIP (الهيماتوبويز الكلوني للإمكانية غير المحددة).
- تسلسل RNA الكامل للورم مع إزالة rRNA.
- تحديد HLA.
- تنبؤ بالببتيدات المحددة لفئة HLA I (المستضدات الجديدة) المتعلقة بالورم الناتجة عن الطفرات من بيانات التسلسل.
- اختيار أكثر المستضدات الجديدة ذات الصلة لفئة HLA I وفئة HLA II.
- تقرير طبي ثاني يتضمن الببتيدات المختارة لصياغة لقاح.
خدمات اختيارية
تحليل الاندماج الجيني بناءً على RNA (CancerFusionRx®) والذي يغطي أكثر من 150 جين للكشف عن الاندماجات وأكثر من 120 إثراء محدد لـ exon-exon مع نقاط كسر معروفة.
تحليلات فحص كميائي هيستولوجي مناعي (IHC): PD-L1، CAR-T cell panel، HLA الفئة I و II التلوين (خارجي).
تحليل التثبيط الميثيلي لمشروط MGMT.

متطلبات العينة القياسية لدينا
مواد عينة إضافية
مصادر مواد العينات الأخرى ممكنة حسب الطلب. يرجى ملاحظة: في حالة جودة العينة غير الكافية أو محتوى الورم، قد تفشل النتائج في التحليل.
إذا كان لديك أكثر من خيار لعينات الأورام، يرجى الاتصال بنا على info@germangeneticsservices.com، وسنساعدك في اختيار العينة الأمثل لمريضك.
للحصول على أقصى دقة، نحن بحاجة إلى النسيج الورمي والطبيعي للوح الأورام الجسمية لدينا.
النسيج الورمي
محتوى الورم على الأقل 20٪
كتلة ورم FFPE:
الحد الأدنى لحجم النسيج: 5 × 5 × 5 ملم (نوع العينة الموصى به)
شرائح أنسجة ورم FFPE:
الحد الأدنى لعدد الشرائح: 10 شرائح بسمك 4-10 ميكرومتر، وحجم النسيج: 5 × 5 ملم
حمض الديوكسي ريبوز النووي الجيني:
أكثر من 200 نانوغرام
نسيج ورم طازج مجمد:
3 × 10 أنابيب cfDNA للتحليل السائل
النسيج الطبيعي
1–2 مل من الدم المضاف إليه EDTA (نوع العينة الموصى به)
حمض الديوكسي ريبوز النووي الجيني (1–2 ميكروغرام)
العملية التشخيصية

هذا ما يجعل خدمة ®CancerNeo لدينا خاصة
تطوير لقاح سرطان شخصي يتطلب أعلى درجات الدقة في تحديد الطفرات الجسدية، فضلاً عن التنبؤ واختيار المستضدات الجديدة لتصميم اللقاح بشكل متسلسل. يقوم ®CancerNeo من CeGaT بتحديد التغيرات الجسدية من خلال التحليل المقارن بين الورم والنسيج الطبيعي. يستند التحليل إلى ®ExomeXtra من CeGaT، وهو أفضل تحضير للأكسوم، وهو الطريقة الأكثر دقة لتحديد الطفرات الجسدية. بالإضافة إلى ذلك، يحدد تسلسل الرنا المستخدم لتحديد الأهداف المحتملة المعبرة عنها بشكل كبير لتصميم اللقاح وهو جزء من عملية اختيارنا استنادًا إلى تجربتنا الطويلة. وبالتالي، يحدد ®CancerNeo بموثوقية المستضدات الجديدة الأكثر وعدًا.
ما هو توقع المستضد الجديدة ؟
يمكن أن تتعرف على المستضدات الجديدة عن طريق الخلايا النابعة من اللمفاوية CD8+ (CTL) والخلايا المساعدة CD4+ لـ T. تتكون المستضدات الجديدة المعترف بها من قبل الخلايا T CD8+ عادةً من 8-12 حمض أميني ويتم تقديمها بواسطة جزيئات HLA الفئة I، في حين أن المستضدات الجديدة المعترف بها من قبل خلايا T المس.
يستخدم خبراء مناعة السرطان لدينا خوارزميات السيليكو المستندة إلى تسلسل الإكسوم وكتابة HLA للتنبؤ واختيار ما يصل إلى 12 حلقة من المستضدات الجديدة المؤهلة والمخصصة لكل مريض. من المتوقع أن تقوم الببتيدات المختارة بتنشيط ليس فقط الخلايا التائية السامة للخلايا ولكن أيضًا الخلايا التائية المساعدة. لذلك، بالإضافة إلى الببتيدات القصيرة (8-12 حمضًا أمينيًا) التي يحتمل أن تكون مرتبطة بجزيئات HLA من الدرجة الأولى، يتم أيضًا تضمين الببتيدات الطويلة (~ 17 حمضًا أمينيًا) التي يحتمل أن تكون مرتبطة بجزيئات HLA من الدرجة الثانية. لتأكيد التعبير عن الحواتم الجديدة المحددة، يتم إجراء بيانات النسخ عن طريق تسلسل الحمض النووي الريبي (RNA) لعينة الورم بالتوازي. في حالات عدم توفر الحمض النووي الريبي (RNA)، يتم استرجاع المعلومات حول تعبير نيوبيتوب من قواعد بيانات التعبير البروتيني
التسلسل الإضافي للوحة الفرعية
الأساس لتحليل ®CancerNeo هو تسلسل الإكسوم بأكمله، حيث يكون من الضروري فهم جميع الطفرات الجسدية لتوقع المستضدات الجديدة. يركز تحضير اللوحة الفرعية المتخصصة للورم الجسدي، وهو أساس خدمتنا التشخيصية ®CancerPrecision، على الجينات المرتبطة بالأورام والتحولات المختارة. وبالتالي، يتم تسلسلها بدقة أعلى. تستند تقريرات الطبيب لدعم اتخاذ قرارات العلاج (®CancerPrecision) على بيانات التسلسل من التحضير الخاص بلوحة الفحص المتخصصة في حين يعتمد تقرير الطبيب للمستضدات الجديدة المتوقعة قابلية استخدام اللقاح الشخصي على بيانات التسلسل من تسلسل الإكسوم بأكمله. يستفيد تقرير ®CancerPrecision من دقة التسلسل الأعلى وإمكانية اكتشاف التحولات المختارة المكثفة بواسطة تسلسل اللوحة الفرعية.

فحص كميائي هيستولوجي مناعي (IHC)
لاكتمال تشخيصنا الجيني، نقدم تنظيم تحليل فحص كميائي هيستولوجي مناعي على عينة الورم بالتعاون مع المختبرات الشريكة. نقوم بتوجيه تقارير الفحص الطبي عند الانتهاء.
PD-L1
تحديد التعبير في نسيج الورم لبروتين 1 المرتبط بالوفاة البرمجية (PD-L1) مهم لاختيار المرضى الذين قد يستفيدون (الأكثر) من العلاج بالمناعة، مثل بيمبروليزوماب.
تحليل ميثيلة مشتق MGMT المحفز
كشف تحليل ميثيلة المحفز MGMT في نسيج الورم مهم لمرضى الورم الدبقي لأنه علامة بيولوجية محتملة للحساسية للعلاج الكيميائي المضاد للألكيل، بما في ذلك تيموزولوميد (TMZ).
HLA الفئة I والفئة II
جزيئات HLA تقدم مستضدات الورم إلى الخلايا T. تحليل تعبير جزيئات HLA هو أداة مفيدة لتصميم استراتيجية العلاج المناعي.
لوحة CAR T cell (GD2، EGFR، IL13Ralpha، CD276، HER2، PSMA، ROR1، CD47)
تعتبر لوحة CAR T cell والتي تكشف عن ثمانية مستضدات مختلفة من الخلايا T المحورة المضادة للورم في التطوير السريري أو ما قبل السريري.
®CANCERFUSIONRX
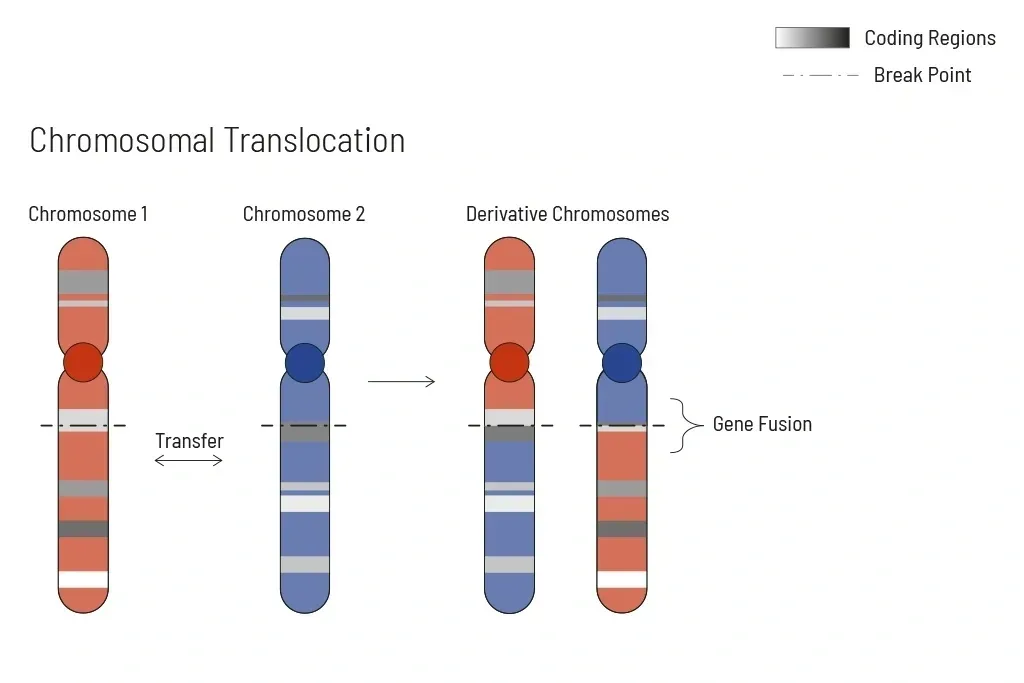
التحديد القائم على الرنا للجينات المندمجة
تحدث إعادة ترتيبات كروموسومية بشكل متكرر في جميع أنواع السرطان. ونتيجة لذلك، يمكن حدوث اندماج الجينات في جينوم السرطان. تعتبر الاندماجات من العوامل الرئيسية في دفع السرطان وبالتالي فهي الأكثر أهمية لاتخاذ قرارات العلاج. لن يكشف الأساليب التقليدية التي تعتمد على تفاعل البوليميرات المتسلسل (PCR) عن اندماج عندما لا يكون الجهاز الآخر معروفًا (ما هو شائع بشكل كبير في الاندماجات التي تؤثر على تيروزين كيناز العصبية النخاعية، NTRK). حتى تحليل النص الكامل للمرسالات الوراثية ليس حساسًا بما يكفي، خاصةً عندما يكون محتوى الورم منخفضًا.
لكشف جميع الاندماجات المعروفة مسبقًا والوصفات الجينية الجديدة والتي تحتوي على خيار علاجي، قمنا بتطوير تحديد مستهدف على أساس الرنا من الجيل القادم. يتضمن التصميم حاليًا أكثر من 150 جينًا لاكتشاف الاندماجات وأكثر من 120 تحسينًا محددًا الإكسون مع نقاط تقاطع معروفة. هذه الطريقة تتفوق على الطرق القائمة على الحمض النووي وأيضًا على النهج الكامل للرنا. نوصي بشدة بإكمال التحليل الجيني للورم باستخدام تحديد الرنا للاندماجات لفهم البيولوجيا الأكثر اكتمالًا للورم.
تحميلات
CeGaT CancerNeo Sample Report (pdf)
